Explicamos o que é pH e quais instrumentos são usados para medi-lo. A escala de pH e exemplos de compostos ácidos, neutros e básicos.

O que é pH?
O pH é uma medida usada para estabelecer o nível de acidez ou alcalinidade de uma solução . O “p” é para “potencial”, por isso o pH é chamado: potencial de hidrogênio.
É expresso como o logaritmo de base 10 negativa da concentração de íons de hidrogênio. A seguinte equação representa esta definição: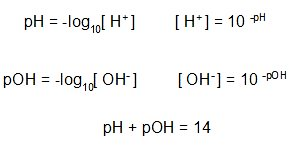
Equação 1: Equações para calcular pH e POH.
Por outro lado, o pOH é uma medida da concentração de íons hidroxila em uma solução . É expresso como o logaritmo de base negativa 10 da concentração de íons hidroxila e, ao contrário do pH, é usado para medir o nível de alcalinidade de uma solução.
Uma informação adicional é que em solução aquosa a 25 ºC, a soma do pH e do pOH é igual a 14.
Veja também: Hidrólise
Qual é a relação entre o nível de acidez e o pH?
As soluções ácidas possuem uma grande quantidade de íons de hidrogênio . Isso significa que eles possuem baixos valores de pH (ver equação 1) e, portanto, seu nível de acidez é alto. Assim, uma solução será mais ácida ou menos ácida dependendo da quantidade de íons de hidrogênio que possui.
Por outro lado, soluções básicas (alcalinas) possuem baixas quantidades de íons hidrogênio . Isso significa que eles possuem valores de pH elevados (ver equação 1) e, portanto, seu nível de acidez é baixo.
A escala de medição de pH
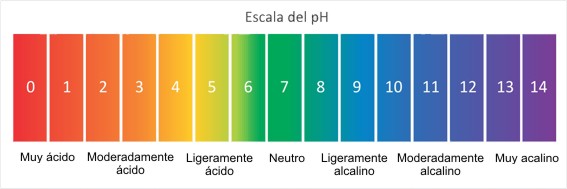
A escala de pH é utilizada para medir o grau de acidez de uma solução e, como o pH está relacionado ao pOH (ver equação 1), conhecendo o grau de acidez de uma solução, também podemos saber seu grau de basicidade.
Assim, a escala de pH vai de 0 a 14. Por exemplo, as substâncias com um valor de pH = 0 são as mais ácidas (menos básicas), aquelas com pH = 7 são neutras e aquelas com pH = 14, são as menos ácidas ( o mais básico).
Exemplos de compostos ácidos, básicos e neutros
Exemplos de compostos ácidos
- Ácidos da bateria . Eles têm valores de pH entre 0 e 1. Seu nível de ácido é tão forte que é prejudicial para a espécie .
- Chuva ácida . É um fenômeno que ocorre devido ao acúmulo de ácidos de fósseis e combustíveis . Essas chuvas podem atingir valores de pH entre 2 e 5 na escala de pH. Quando o pH se aproxima de 2, pode causar a morte de peixes, plantas e outras espécies . Quando o pH se aproxima de 5, ele produz menos danos, mas ainda afeta a vida aquática e terrestre.
- Suco de limão. Possui valores de pH entre 2 e 3.
- Café. Possui um valor de pH = 5 ou valores muito próximos.
Exemplos de compostos neutros
- Sangue
- Leite
Exemplos de compostos básicos
- Leite de magnésia. Na tabela de pH está localizado entre os valores 10 e 11. Este produto é para consumo
- Água sanitária ou cloro. Possui valores de pH em torno de 13. É utilizado para limpar a casa, banheiros, cozinha e tem o poder de descolorir roupas.
Como o pH é medido?

A maneira de distinguir entre um composto ácido e um básico é medindo seu valor de pH. Hoje, existem vários métodos para medir o pH de uma substância.
- Usando indicadores ácido-base. Indicadores são compostos que mudam de cor conforme muda o pH da solução em que são encontrados. Por exemplo, a fenolftaleína é um líquido que fica rosa se adicionado a uma base e torna-se incolor se adicionado a um ácido. Outro exemplo é o papel de tornassol: se um fragmento é imerso em uma solução ácida, torna-se vermelho-alaranjado, e se imerso em uma solução básica escurece, adquirindo uma coloração azulada. Existem também alguns tipos de papel de tornassol com escalas de cores mais específicas que indicam valores de pH mais precisos.
- Usando um potenciômetro ou medidor de pH. É um equipamento eletrônico que nos fornece diretamente o valor de pH de uma solução. Medir o pH com este equipamento é mais preciso do que com papel de tornassol.
O que são soluções de buffer ou buffers?
Soluções tampão ou tampões são soluções que têm a propriedade de manter constante o pH de uma solução , mesmo quando certas quantidades de ácido ou base são adicionadas .
As soluções tampão são de vital importância na regulação do pH de diversos processos biológicos, pois para que muitos deles ocorram é necessário que o pH do meio em que ocorrem se mantenha constante.