Explicamos o que é calor específico e quais são suas unidades. Além disso, as fórmulas usadas para calculá-lo e alguns exemplos.
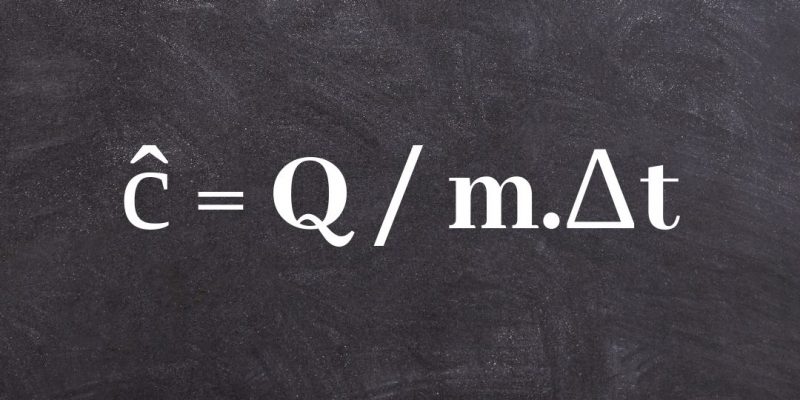
O que é calor específico?
Em física , calor específico (também chamado de capacidade térmica específica ou capacidade de calor específica ) é entendido como a quantidade de calor necessária para que uma unidade de uma substância aumente sua temperatura em uma unidade de grau Celsius.
O calor específico varia de acordo com o estado físico da matéria , ou seja, é diferente se a matéria está no estado sólido , líquido ou gasoso, pois sua estrutura molecular particular afeta a transmissão do calor no sistema de partículas . O mesmo acontece com as condições de pressão atmosférica: quanto maior a pressão , menor o calor específico.
Veja também: Propriedades da matéria
Unidades de calor específicas
Como no Sistema Internacional de medidas a unidade de calor é joules (J) , o calor específico é expresso neste sistema em joules por quilograma e por kelvin (J.Kg -1 .K -1 ).
Outra forma comum de medição envolve o uso de calorias por grama e grau centígrado (cal.g -1 . ° C -1 ), e em países ou áreas que usam o sistema anglo-saxão, é medida com BTU por libra. e por grau Fahrenheit. Esses dois últimos, fora do SI.
Fórmulas de calor específicas
A fórmula mais comum para calcular o calor específico de uma substância é:
ĉ = Q / m.Δt
onde Q representa a transferência de energia térmica entre o sistema e seu entorno, m a massa do sistema e Δt a variação de temperatura a que está sujeito.
Assim, o calor específico ( c ) a uma dada temperatura ( T ) será calculado da seguinte forma:
c = lim (Δt → 0). Q / m.ΔT = 1 / m. dQ / dT
Quanto mais alto o calor específico de uma substância em relação a um determinado suprimento de calor, menos sua temperatura irá variar. Por exemplo, preferimos usar uma colher de pau para cozinhar e não de alumínio, pois o calor específico da madeira é consideravelmente maior do que o do alumínio.
Pode servir a você: Transferência de calor
Exemplos de calor específico

Um exemplo simples de calor específico é o da água . É necessária uma caloria para aumentar um grau Celsius por grama de água à temperatura ambiente, ou seja, o calor específico da água é 1 cal.g -1 . ° C -1 . Por outro lado, são necessários 0,5 calorias para aumentar a temperatura do gelo em um grau até -5 ° C.
A água é a substância comum com maior calor específico e por isso desempenha um papel muito importante na regulação da temperatura do planeta .
Outros registros de calor específicos são:
- Alumínio. 0,215 calorias por grama por grau Celsius
- Cobre . 0,0924 calorias por grama por grau Celsius
- Ouro. 0,0308 calorias por grama por grau Celsius
- Ferro. 0,107 calorias por grama por grau Celsius
- Silício. 0,168 calorias por grama por grau Celsius
- Potássio. 0,019 calorias por grama por grau Celsius
- Copo. 0,2 calorias por grama por grau Celsius
- Mármore. 0,21 calorias por grama por grau Celsius
- Madeira. 0,41 calorias por grama por grau Celsius
- Álcool etilico. 0,58 calorias por grama por grau Celsius
- Mercúrio. 0,0033 calorias por grama por grau Celsius
- Azeite de oliva. 0,47 calorias por grama por grau Celsius